ה-FDA, רשות המזון והתרופות האמריקאית, עשויה - או עלולה - לעבור בחודשים הקרובים שינויים מפליגים. ראש ה-FDA הוא מינוי פוליטי ישיר של נשיא ארה"ב, המשקף את תפיסת עולמו של הנשיא בענייני בריאות וכלכלת בריאות. טראמפ כבר השפיע על רשות המזון והתרופות בכך שעצר גיוס עובדים לרשות, עד שימנה לה מנהל חדש אשר יגייס אנשים שיפעלו לפי תפיסתו. גורמים ב-FDA אומרים כי הקפאת גיוס העובדים משבשת את פעילות הרשות.
ביום שלישי האחרון ערך טראמפ פגישה עם בכירי תעשיית התרופות כדי לתאר להם את הרפורמות הצפויות. טראמפ הסביר כי בדעתו לבצע ב-FDA דה-רגולציה "ברמה שאיש לא ראה בעבר", ועם זאת עדיין להעניק הגנה "עצומה" לציבור מפני תרופות מסוכנות או לא יעילות.
בינתיים חתם טראמפ על הוראה כללית לרשות, לבטל שתי רגולציות בעבור כל רגולציה חדשה שמטמיע הארגון. מי שמייעץ לנשיא בתחום זה הוא פיטר תיל, איש הון סיכון המוכר בין היתר כמייסד פיי פאל וכמשקיע החיצוני הראשון בפייסבוק.
כאמור, לא כולם מרוצים מגישה זו. גורמים רבים מתוך תעשיית הפארמה ובכירי FDA לשעבר, טוענים כי ה-FDA כבר היום היא רשות מהירה ביותר, וכי מהירות רבה יותר עלולה להיות מסוכנת.
"לתמוך במו"פ אפקטיבי"
עבודת הרשות הואטה משמעותית בסוף העשור הקודם (ראו גרף) לאחר משבר ה-VIOXX, תרופה שהוסרה מן המדפים לאחר שגרמה להתקפי לב. לאחר החקירות בעקבות הפרשייה הפכה הרשות זהירה והססנית, אולם שורה של מסלולי אישור חדשים ורוח חדשנית שהוטמעו ברשות בשנים האחרונות, וכן תקצוב נוסף ודדליינים בחוק המגבילים את התקופה עד אישור, שינו זאת והובילו למספר שיא של אישורי תרופות בשנים האחרונות, למעט 2016 שאכן היתה קצת חלשה.
מרק בר מקללן כיהן כראש ה-FDA בשנים 2002-2004, והיה מינוי של הנשיא הרפובליקני ג'ורג' וו. בוש. הוא גם כיהן כראש ה-CMS (הרשות שאחראית על סל הבריאות האמריקאי) בשנים 2004-2006, גם כן תחת הנשיא בוש. בתפקידו זה עזר להטמיע את רפורמת PartD של הביטוח הממשלתי, אשר מכסה תשלום עבור תרופות (קודם לכן הביטוח הממשלתי כיסה רק תשלום עבור שהות בבית חולים ועבור הטיפולים הניתנים שם).
מקללן הוא רופא פנימאי, וכיום הוא עוסק במחקר וייעוץ בתחום כלכלת הבריאות. השבוע הגיע לביקור ראשון בישראל על מנת להשתתף בוועידה השנתית הבינלאומית השלישית למדעי החיים שמארגנת קבוצת שטיר, שתחל מחר בתל אביב.
"תחום הבריאות בארה"ב עובר תהליכים חשובים מאוד עוד לפני ההתערבות של הנשיא טראמפ", הוא אומר בראיון בלעדי ל"גלובס". "בממשל הקודם נחקק חוק בשם 21st Century Cures, שאחת ממטרותיו היא להפוך את ה-FDA ליעיל יותר ולתמוך במו"פ יותר אפקטיבי. כשאומרים היום שתהליך ה-FDA הוא יקר וממושך, הכוונה איננה לכך שהבוחנים מטעם ה-FDA הם שעובדים לאט ולוקחים את הזמן - כיום תרופות שנחשבות לחשובות ומצילות חיים ומוערכות במסלול המהיר, תקבלנה תשובה תוך חצי שנה בלבד - אלא שתהליך עריכת הניסויים ובניית התיק להגשה ל-FDA, דורש את הזמן.
"המטרה של החקיקה החדשה היא לשנות את האופן שבו בכלל חוקרים יעילות של תרופות. הכוונה היא לאפשר השגת מידע מוצלח לגבי בטיחות ויעילות התרופה, באופן מהיר יותר מן הקיים היום. כך למשל, ניתן יהיה לאשר תרופות לא רק כאשר מוכיחים שינוי בבריאות של נבדקים בניסויים המוניים, עניין שמורכב יותר להראות, אלא גם כאשר מראים השפעה של התרופה על סמנים ביולוגיים שידועים כמשפיעים על הבריאות (כך למשל, חברות התרופות יצטרכו להראות הורדת סוכר בדם, ולא מניעת קטיעת רגל בסוכרתיים, או ירידה בכולסטרול ולא בהכרח הארכת חיים של חולי לב, או עליה ברמות החיסוניות ולא הארכת חיים בפועל של חולי איידס).
"שינוי נוסף הצפוי תחת הרפורמה הזו, הוא הכללה של רצונות והעדפות המטופל בניסויים הללו. כלומר, אם עד היום רופאים קבעו מהו היעד של הניסוי (ולפעמים הם קבעו כי 'שיפור בשאלון ההרגשה הטובה' של החולה הוא היעד, אבל לפעמים קבעו יעדים אחרים), הרי שכעת אנחנו נשאל גם את החולים מה לדעתם להיות יעד הניסוי, כדי שניתן יהיה לומר שהתרופה היא יעילה עבורם".
כך ייתכן למשל שחולים ידגישו יעדים הקשורים במניעת כאב ושיפור תפקוד, בעוד הרופאים הדגישו יעדים כמו תוחלת חיים ושמירה על שלמות רקמות.
מקללן: "שינוי נוסף הוא להפוך את הניסויים ליותר אדפטיביים: לשנות ניסויים בעיצומם בהתאם לתוצאות מן החולים הראשונים, לאשר מוצרים במהירות אבל לקהל חולים קטן ולחקור את התרופה בקהל קטן זה אבל בשימוש שהוא לא במסגרת ניסוי אלא יותר בעולם האמיתי, ללמוד כמה שאפשר מרשומות רפואיות קיימות ולא רק מניסויים שנערכים במיוחד".
אחד הכללים שקבע חוק 21 century cures הוא שלא בהכרח חייבים להשיג אישור של המטופל אם מעוניינים לערוך ניסוי על מידע שנאסף ממנו, ואם הניסוי אינו פוגע בבריאותו או בפרטיותו. זהו שינוי מהותי מאוד לעומת הגישה שרווחה עד כה, שלפיה כל שימוש מחקרי בנתוניו של מטופל מחייב את אישור המפורש לכל ניסוי וניסוי שנערך בהם.
הזדמנויות רבות להכניס רפורמות
"אחד הדברים החשובים ברפורמה הוא להכשיר את אנשי ה-FDA לגישות החדשות הללו. אנחנו עדיין מנסים להבין מה זה אומר להיות FDA יותר יעילה".
- האם הקפאת הגיוסים ל-FDA משפיעה על היכולת להטמיע את המהפיכות הללו?
"תקנת 'דמי השימוש' הגובה סכום מסוים מחברות שמגישות מוצרים לאישור, עוזרת למימון הרשות וגם לגיוס עובדים.
"לדעתי הקפאת הגיוס כעת לא תעכב אותן באופן משמעותי בינתיים, משום שהיא מכילה כמה הסתייגויות אשר מאפשרות לגייס עובדים בתחומים בוערים וכן של עובדים שהם כבר היום עובדי מדינה".
מכלול הרפורמות הללו יכול להיות מעט מבלבל עבור התעשייה. "אחת מהדרישות החשובות לגבי הרגולציה של ה-FDA, היא יציבות, ודאות. אמנם לפעמים חייבים לשנות מסלול רישום לתרופה בגלל שינויים במדע, או במוצר, אבל ככל שיש יותר ודאות, זה מוריד למעשה את הסיכון ולכן את העלות של פיתוח התרופה".
- אז נראה שה-FDA כבר הולך בכיוון שטראמפ רוצה, תחת החוק מתקופת אובמה.
מקללן: "ישנן הזדמנויות רבות נוספות לרפורמות, למשל בחיפוש אקטיבי אחרי אירועי בטיחות תרופות לאחר השקת התרופה, באמצעים אלקטרוניים. היום הרופא מדווח על האירועים האלה ידנית ולוקח הרבה יותר מדי זמן לאתר אותם.
"בזכות השיפור בדרכי המעקב שלנו אחרי הבריאות המטופלים ובזכות שיפור באלגוריתמים שנועדו להתריע על בעיה אפשרית תוך מיעוט התראות שווא, אנחנו יכולים לשפר מהותית את המעקב אחרי אירועי בטיחות כשהתרופה כבר בשוק. הדבר נכון במיוחד לאיתור בעיות בטיחות של תרופות כשמטפלים בחולים עם יותר ממחלה אחת, שלרוב מוחרגים מניסויים קליניים. כדי שנוכל באמת לעשות את הרפורמה הזו, נצטרף שיתוף פעולה בין גורמים מהממשלה לבין גורמים מהתעשייה".
תשלום עבור תרופות: המחיר נקבע לפי ההתוויה
כאמור, מקללן כיהן בנוסף לתפקידו כראש ה-FDA, גם כראש ה-CMS. בין הגופים הללו יש היום ממשק. "חברות מעוניינות לדעת מראש כשהמוצר שלהן נכנס לשוק, לא רק האם ניתן יהיה לשווקו אלא גם האם חברות הביטוח הממשלתיות והפרטיות צפויות לשלם עבורו (כלומר האם הוא ב"סל הבריאות" שלהן). לפעמים, כדי לקבל אינדיקציה לכך, החברות כוללות כבר בתוך ניסויי היעילות שלהם גם השוואות שנועדו להראות לחברות הביטוח כמה כסף ניתן לחסוך באמצעות התרופה, אבל זה לעולם לא יהיה מעניינו של ה-FDA. זה לא חלק מן החזון שלו.
"אלא שחלק מסוגיית גובה התשלום תיקבע לפי ההתוויה שה-FDA מעניק לתרופה, כלומר ההגדרה בדיוק לאילו קהלי חולים המוצר מיועד, וכן רמת האכיפה שלו לגבי השיווק של המוצר לחולים שאינם כלולים בדיוק בקהלים הללו".
- גם מבוטחים ממשלתיים מקבלים היום את התרופות שלהם דרך חברות ביטוח פרטיות, בסבסוד ממשלתי. העלויות של התרופות הניתנות כך היו אחד ממוקדי הדיון החמים ביותר לקראת הבחירות האחרונות. מה עמדתך בעניין? האם חברות התרופות אכן הגזימו בתמחור?
"תמחור תרופות בארה"ב הוא עניין מסובך. אחד השינויים המשמעותיים שקרו בשנים האחרונות, כשה-CMS החל לממן תרופות, הוא שהחולים שילמו על מחיר קטלוגי של תרופה, והם שילמו מכיסם עד תקרת השתתפות עצמית מסוימת, בעוד המבטחים קיבלו הנחה על הזמנתם ובעצם לא שילמו את המחיר הקטלוגי. כך, החולים והממשלה בעצם סבסדו את חברות הביטוח. כדי להילחם בתופעות הללו, יתוקנו כנראה תקנות המחייבות שקיפות רבה יותר לגבי המחירים המשולמים על ידי חברות הביטוח לחברות התרופות.
"בתחום הגנריקה, המחירים צריכים להיות נמוכים בגלל תחרות בין חברות, אך הם לא היו כאלה משום שמספר חברות מצאו את עצמן מונופולים בתחומים מסוימים גם אחרי תפוגת הפטנט. התגובה של הממשלה היא לאשר יותר תרופות גנריות יותר בקלות, כדי שהתחרות בתחום הזה תגדל."
- לאחרונה התעוררה סערה כשטראמפ אמר כי יאפשר לחברות התרופות להתמקח על המחירים.
"זה רלוונטי לתרופות הניתנות בבתי החולים ולתרופות ביולוגיות הניתנות במרפאות. סביב מוצרים אלו אין תחרות, וחברת התרופות בעצם נוקבת במחיר והממשלה משלמת אותו. כעת בתחום הזה מנסים היום לעודד תחרות בכל מקום שאפשר, גם אם המוצרים לא לגמרי זהים. לכשייכנסו תרופות ביוסימילר, שהן בעצם גנריקה של תרופות ביולוגיות, יגדל כוח המיקוח של הממשלה".
מקללן היה גם מהחלוצים בפתיחת המבטחים הממשלתיים למודלים של תשלום עבור הצלחה. "זה אחד הדברים שאדבר עליהם בכנס - מודלים שבהם המבטח משלם כשבריאות המטופל משתפרת ולא בכל פעם שהוא נוטל תרופה. אולם כדי שנגיע לכדי כך, צריך לשפר את איסוף וניתוח המידע על יתרונות וסיכונים אצל חולים מסוימים".
- ה-CMS כבר ערוך לעבוד עם מודל כזה?
"כן, זה מתחיל לקרות, ונחתמו חוזים כאלה בתחום הפחתת הכולסטרול (שהוא מדיד בקלות) ובתחום מניעת סיבוכים בקרב חולי לב. גישה כזו מחייבת גם את חברת התרופות לעבוד עם הרופאים כדי לוודא כי החולה מטופל כראוי ובאמת מקבל את מלוא התועלת מהתרופה.
"אחד התחומים העיקריים שאני עובד עליהם במרכז למדיניות בריאות על שם מרגוליס באוניברסיטת דיוק, הוא הכשרה של גורמים שונים במערכת להיות מסוגלים להתמודד עם מודלים כאלה. לשם כך עלינו להעשיר את קבוצת הטיפול בחולה באחיות ובעובדים סוציאליים שתפקידם לוודא כי הטיפול הרפואי מגיע אל המטופל בצורה הטובה היותר. הבעיה העיקרית כאן היא שהיום חברות הביטוח לא משלמות לבעלי התפקידים הללו. צריך להראות להן מדוע זה כדאי".
- האם הבדיקות של ה-FDA יוחלפו בביקורת צרכנים?
בין השמות שהוזכרו בתקשורת האמריקאית ככאלה שטראמפ בוחן לתפקיד ראש ה-FDA הם ד"ר סקוט גוטליב, בעבר סגן ראש הרשות; ג'ים אוניל, שותף בקרן פרייבט אקוויטי שמתח בעבר ביקורת נוקבת על הרשות; וג'וזף גולפו, שניהל בעבר חברה שביקשה לקבל אישור מן הרשות לתרופה חדשה, ואח"כ כתב ספר שכותרתו 'משבר החדשנות: כיצד ה-FDA ו-וול סטריט פוגעות בהתקדמות הרפואית".
גולפו תומך בהקלות בתהליך ה-FDA מן הסוג של מעקב אחרי סמנים ביולוגיים במקום הגישה הנוכחית המבקשת לראות שינויים בתסמינים הרפואיים של החולה (למשל סוכר בדם לעומת קטיעת רגל). "הבעיה היא שלפעמים הסמן הביולוגי טועה, ובזמן שאנחנו מלעיטים את המטופל בתרופה שאולי יש לה תופעות לוואי והיא עוזרת לו רק 'על הנייר', אולי היינו יכולים לתת לו תרופה שתעזור לו באמת", אומרים המבקרים.
בנייר עמדה מ-2016 ציין גולפו כי חברות הביטוח עדיין תוכלנה לדרוש ניסויים מעמיקים יותר כדי לבדוק עבור אילו תרופות הן מעוניינות לשלם. אולם בעוד ה-FDA מחויב היום לבחון ניסויים ולהביע דעתו עבור כל תרופה, חברות הביטוח יעשו זאת רק במקרים שבהם זה משתלם, וייתכן כי דווקא חולים במחלות נדירות יסבלו מכך.
אוניל לוקח את הרעיון הזה צעד קדימה ומדבר על האפשרות של "Yelp לתרופות". רעיון זה, שתואם רעיונות שהשמיע בעבר פיטר תיל, הוא שה-FDA יאשר את כל התרופות שהן בטוחות לשימוש, והשוק יקבע באופן חופשי אילו תרופות הן היעילות ביותר, על בסיס ביקורת צרכנים כמו באתר ביקורת המסעדות "יילפ".
גורמים בתעשיית התרופות מזועזעים מהרעיון של "יילפ לתרופות", כתחליף לבדיקת היעילות של ה-FDA. ראשית, הם אומרים, אין דבר כזה "תרופה בטוחה". לכל התרופות ישנן תופעות לוואי, ואת הבטיחות יש לקבוע ביחס ליעילות - האם התועלת עולה על הפגיעה? מעבר לכך, הם לא מאמינים שהציבור יכול לתת ביקורת משמעותית על תרופה שתחליף את הבדיקות המקצועיות. "רק 2% מהאוכלוסיה מבינים בכלל מה אנחנו עושים", אמר בכיר מתוסכל מן הרשות. "מה יודע נוטל התרופה הממוצע על הרעילות ארוכת הטווח שלה או על אופן הפירוק שלה על ידי הגוף לעומת טיפולים מתחרים?"
מקללן מדגיש כי לא כל כך מהר תוותר ה-FDA על הסמכות שלה לבחון יעילות. "זה לא עניין שניתן לשנותו באמצעות תקנות, אלא אך ורק באמצעות חקיקה". הוא אומר. "אנחנו גם לא נשנה את האופן שבו יעילות מוגדרת. מה שישתנה הוא אולי, כאמור, האופן שבו אנחנו בודקים את אותה יעילות. "במקביל בהחלט יש מקום ל'ילפ' לתרופות, כמסלול נוסף ולא במקום הבדיקות של אנשי המקצוע. ה-FDA הולך להיות הרבה יותר מבוסס צרכן".
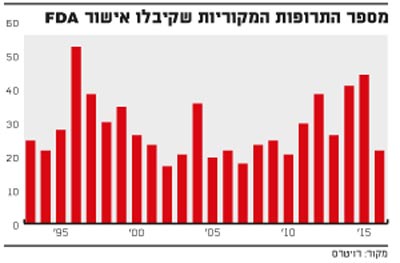
מספר התרופות המקוריות